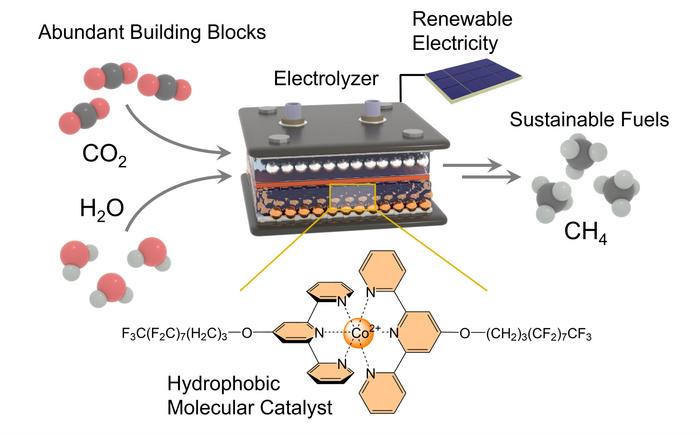
Roma – Un innovativo catalizzatore in grado di trasformare anidride carbonica ed acqua in metano in modo altamente efficiente utilizzando l’elettricità. E’ quanto sviluppato dai ricercatori dell’Università di Bonn e dell’Università di Montreal che hanno pubblicato i loro risultati su Nature Chemistry. “Abbiamo usato l’elettricità come forza motrice”, spiega il Prof. Dr. Nikolay Kornienko. “Utilizzando elettricità da fonti rinnovabili, possiamo produrre metano che non contribuisce al riscaldamento globale”. “La produzione di metano, che ha la formula chimica CH4, è impegnativa perché è necessario effettuare una reazione tra un gas e un liquido”, afferma Kornienko. In questo caso, stiamo parlando di anidride carbonica (CO2) e acqua (H2O). I ricercatori hanno utilizzato un elettrodo a diffusione di gas per unire questi due partner. Nella reazione, è necessario separare i due atomi di ossigeno (simbolo chimico: O) dall’atomo di carbonio (C) e sostituirli con quattro atomi di idrogeno (H). L’idrogeno è ricavato dall’acqua. Il problema di questo processo è che l’acqua preferirebbe di gran lunga subire un’altra reazione e si dividerebbe in idrogeno e ossigeno non appena esposta a una corrente elettrica. “Questa è una reazione concorrente che dobbiamo evitare”, sottolinea l’assistente di Kornienko, Morgan McKee, che ha condotto una gran parte degli esperimenti. “Altrimenti, ci impedirebbe di produrre metano. Pertanto, dobbiamo impedire all’acqua di entrare in contatto con l’elettrodo. Allo stesso tempo, abbiamo ancora bisogno dell’acqua come partner di reazione”. È qui che entra in gioco il catalizzatore di nuova concezione, depositato sull’elettrodo. Esso assicura soprattutto che l’anidride carbonica reagisca più prontamente e rapidamente per produrre metano. Ciò avviene grazie al suo cosiddetto “centro attivo” che trattiene l’anidride carbonica e, in parole povere, indebolisce anche i legami tra l’atomo di carbonio e i due atomi di ossigeno. Questi atomi di ossigeno vengono poi gradualmente sostituiti da quattro atomi di idrogeno nella fase successiva. Il catalizzatore ha bisogno di acqua in questa fase del processo. Tuttavia, deve anche tenerla a distanza per evitare reazioni collaterali indesiderate. “Per raggiungere questo obiettivo, abbiamo legato lunghe catene laterali molecolari al centro attivo”, spiega il Prof. Kornienko, che è anche membro della Transdisciplinary Research Area “Matter” presso l’Università di Bonn. “La loro struttura chimica respinge l’acqua”. (30Science.com)
Gianmarco Pondrano d'Altavilla
Catalizzatore innovativo produce metano utilizzando l’elettricità
(4 Ottobre 2024)
Gianmarco Pondrano d'Altavilla