Roma – Nella lunga battaglia per creare un vaccino efficace contro l’HIV, gli scienziati hanno fatto un importante passo avanti. Un nuovo studio dimostra che una serie di vaccini può indurre il sistema immunitario a produrre anticorpi potenti in grado di bloccare un’ampia gamma di ceppi di HIV, compresi quelli che sono tipicamente i più difficili da bloccare. Pubblicata su Immunity, la ricerca nasce da una collaborazione guidata da scienziati di Scripps Research e del Karolinska Institutet svedese. I loro risultati rappresentano una solida dimostrazione che gli anticorpi ampiamente neutralizzanti (bNAb), a lungo considerati un obiettivo chiave per la vaccinazione contro l’HIV, possono essere indotti con successo nei primati non umani. Indica inoltre un nuovo bersaglio sulla proteina spike dell’HIV che i futuri anticorpi potrebbero essere in grado di legare con successo per bloccare il virus. “Ciò che distingue questo lavoro è che non abbiamo solo visto i primi segnali di una risposta promettente; abbiamo effettivamente isolato anticorpi funzionali ampiamente neutralizzanti e individuato esattamente dove si legano sulla superficie del virus”, afferma l’autore senior Richard Wyatt , professore presso il Dipartimento di Immunologia e Microbiologia presso Scripps Research. “Questo ci dice non solo che l’approccio funziona, ma anche esattamente perché funziona”. Poiché l’HIV muta rapidamente e ci sono letteralmente milioni di ceppi diversi che circolano negli esseri umani in tutto il mondo, gli scienziati hanno concentrato i loro sforzi di ricerca sulla creazione di vaccini in grado di stimolare l’organismo a produrre bNAb che riconoscono simultaneamente molti ceppi. Mentre alcune persone producono spontaneamente bNAb dopo l’esposizione all’HIV, creare un vaccino che induca in modo affidabile bNAb nei primati non umani o negli esseri umani è stata una sfida. Nel nuovo lavoro, Wyatt e il suo team hanno inizialmente progettato un imitatore della proteina spike dell’HIV, una sezione chiave del meccanismo di azione dell’HIV che gli anticorpi prendono di mira per bloccare l’infezione. A differenza dei progetti precedenti, i nuovi “imitatori della spike” non si disgregano dopo l’iniezione e assomigliano molto alla struttura della proteina spike dell’HIV. Il gruppo ha quindi adottato una strategia vaccinale in due fasi. In primo luogo, ha preparato il sistema immunitario con una versione del mimetico della proteina Spike priva di molecole di zucchero chiave, che normalmente rivestono la proteina e ne rendono più difficile il riconoscimento. Questo ha contribuito a rivelare una regione critica e conservata della proteina Spike: il sito di legame CD4, dove la proteina Spike si lega alle cellule immunitarie umane. Dopo due dosi sequenziali del vaccino di innesco, sono stati somministrati cinque richiami, ciascuno a circa dodici settimane di distanza. Questa serie di richiami di proteine spike di diversi ceppi di HIV – ora con il loro rivestimento zuccherino intatto – ha rieducato il sistema immunitario a riconoscere la stessa regione anche quando era parzialmente nascosta.
La sequenza deliberata dei vaccini, affermano i ricercatori, è stata la chiave del successo. “Non stavamo vaccinando a caso”, afferma Javier Guenaga, ricercatore senior presso Scripps Research e co-primo autore del nuovo articolo. “Si è trattato di un approccio razionale, basato sulla struttura, per ottenere i giusti tipi di anticorpi”. L’approccio ha dato i suoi frutti. Diversi modelli animali vaccinati hanno prodotto anticorpi in grado di neutralizzare i ceppi di HIV di “livello 2”, tra i più difficili da bloccare. Da un modello animale, i ricercatori hanno isolato una famiglia di anticorpi, denominata LJF-0034, che ha neutralizzato quasi il 70% di un campione globale di 84 ceppi di HIV.
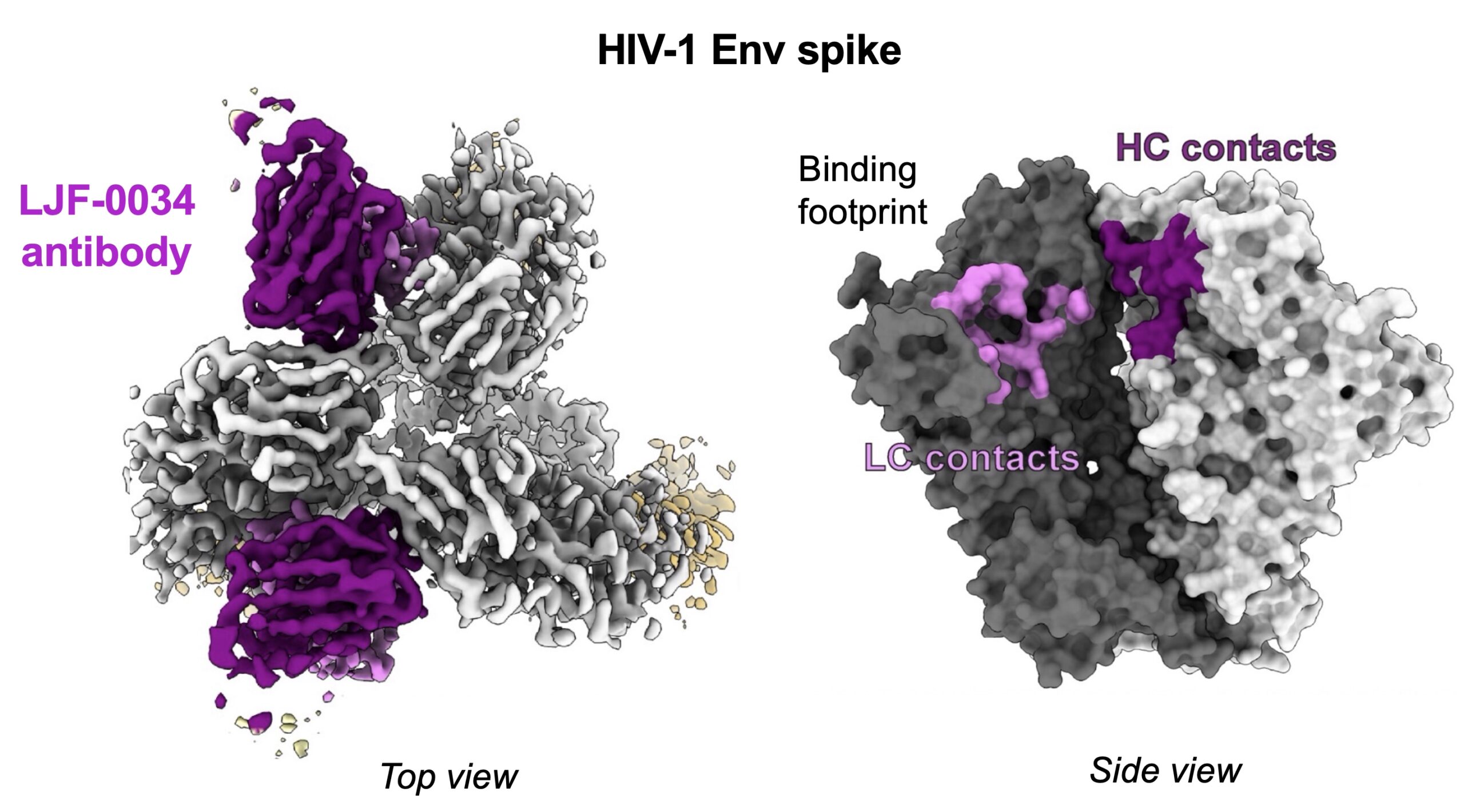
“È incredibilmente entusiasmante vedere un vaccino generare questo tipo di diffusione nei primati non umani”, afferma Shridhar Bale, ricercatore senior e coautore principale dello studio. “E non si tratta di un caso isolato. Abbiamo osservato risposte mirate a questo sito in diversi animali”. Il gruppo ha poi dimostrato che anticorpi come LJF-0034 si legano a un sito del virus precedentemente non descritto, creando un ponte tra due sezioni della proteina spike. La ricerca futura potrà contribuire a guidare lo sviluppo di ulteriori vaccini mirati a questo nuovo, promettente sito. Wyatt afferma che il suo team vorrebbe ottimizzare il vaccino in modo che possa indurre in modo affidabile risposte simili a quelle di LJF-0034 in una percentuale maggiore di riceventi. In definitiva, un regime vaccinale efficace contro l’HIV comprenderà probabilmente una combinazione di vaccini che producono diversi bNAb, tutti agenti insieme. “Siamo ben lontani dall’essere un vaccino definitivo”, afferma Wyatt. “Ma avere un nuovo obiettivo altamente efficace è incredibilmente entusiasmante e ci aiuterà a dare forma ai nostri sforzi futuri”. Un candidato vaccino utilizzato in questo studio è già in fase di sperimentazione clinica in una sperimentazione clinica di fase 1, i cui primi risultati sono attesi a breve. In tale sperimentazione, i partecipanti umani ricevono la stessa proteina spike (priva di molecole di zucchero) utilizzata come vaccino di innesco in questo studio.(30Science.com)