Roma – Un farmaco assunto per via orale che ripristina le cellule sane del sangue potrebbe essere un potenziale trattamento per la cura della malattia falciforme. Il farmaco sperimentale, descritto oggi su Science, offre la speranza che la malattia falciforme possa un giorno essere ampiamente ed economicamente trattata con una semplice pillola. L’anno scorso, la Food and Drug Administration, o FDA, statunitense ha approvato due procedure di terapia genica che possono trattare e, in alcuni casi, essenzialmente curare la malattia falciforme, una malattia genetica del sangue che provoca dolore e anemia in milioni di persone e che ancora oggi uccide circa 375.000 persone in tutto il mondo ogni anno. Ma questi trattamenti innovativi richiedono una rischiosa chemioterapia e costano circa 2 milioni di dollari a persona, rendendoli inaccessibili alla stragrande maggioranza dei malati. A differenza di una terapia genica una tantum i cui benefici potrebbero durare decenni, il nuovo composto, per cui non sono ancora iniziati i test di sicurezza sugli esseri umani, dovrebbe essere assunto periodicamente per tutta la vita. “Sembra promettente”, ha affermato Lewis Hsu, ematologo pediatrico dell’Università dell’Illinois di Chicago, che non è stato coinvolto nella nuova ricerca. “Tuttavia – ha avvertito Hsu – ci sono una serie di trattamenti farmacologici per la malattia falciforme che funzionano nei topi e nelle cellule, ma che non hanno funzionato nelle persone”. Nella malattia avviene una mutazione che fa sì che i globuli rossi, normalmente a forma di disco, assumano la caratteristica forma a mezzaluna e si incollino tra loro, ostruendo i capillari, danneggiando i tessuti e scatenando episodi di forte dolore. Una delle due terapie recentemente approvate utilizza un virus ingegnerizzato per inserire copie di una versione modificata del gene dell’emoglobina adulta nelle cellule staminali del paziente stesso. Queste cellule programmate vengono poi restituite alla persona dopo che la chemioterapia ha eliminato le cellule staminali del sangue esistenti. Anche l’altra terapia approvata modifica le cellule staminali del sangue del paziente, ma utilizza il sistema di editing genico CRISPR per bloccare il gene di una proteina chiamata BCL11A, che negli adulti reprime la produzione di una forma di emoglobina utilizzata dai feti. Durante l’infanzia, questa emoglobina fetale viene normalmente ridotta perché i bambini passano a produrre la versione adulta. Quindi, quando CRISPR spegne il gene BCL11A, ripristina la produzione di emoglobina fetale nelle cellule staminali del sangue, aiutando i pazienti affetti da falcemia. Ma, i costi elevati e la complessità della terapia genica hanno reso difficile capire come l’uno o l’altro approccio possa funzionare nei paesi a basso reddito, soprattutto in Africa, dove risiede la maggior parte delle persone affette dalla malattia falciforme. “Le aziende farmaceutiche sono da tempo alla ricerca di farmaci in grado di attivare l’emoglobina fetale negli adulti”, ha detto Pamela Ting, ricercatrice in ematologia presso Novartis. “Nel 1998, la FDA ha approvato un farmaco chiamato idrossiurea, che si è rivelato in grado di aumentare modestamente la produzione di emoglobina fetale”, ha continuato Ting. “Ma – ha aggiunto Ting – il farmaco può anche sopprimere la proliferazione delle cellule staminali del midollo osseo, causando anemia e altri effetti collaterali, un problema che ha messo in crisi anche molti altri farmaci contro la falcemia”. “L’intero settore si è scontrato con questo problema”, ha osservato Ting. Una squadra di ricerca, guidata da Ting e Bradner, ha recentemente cercato composti che si legano a una proteina chiamata cereblon, nota per etichettare altre proteine per la distruzione da parte del sistema naturale di riciclaggio delle proteine delle cellule. La speranza iniziale era quella di trovare un composto che aiutasse il cereblone a marcare la proteina BCL11A, ripristinando così la produzione di emoglobina fetale. Gli scienziati hanno esaminato una libreria di 2814 molecole che si legano a cereblon e le hanno somministrate ai globuli rossi immaturi, scoprendone una, chiamata dWIZ-1, che ha aumentato la produzione di emoglobina fetale. Ma inaspettatamente non aveva come bersaglio BCL11A, ma si agganciava a un’altra proteina regolatrice del gene chiamata WIZ, che non era nota per essere coinvolta nel controllo dei livelli di emoglobina fetale. Un ulteriore perfezionamento del composto ha prodotto il dWIZ-2, che secondo il gruppo di ricercatori ha aumentato la produzione di emoglobina fetale nei globuli rossi da un valore di base dal 17% al 45%. “Quest’ultimo è un livello che produrrebbe globuli rossi funzionali se tradotto nell’uomo”, ha spiegato Bradner. Il composto ha funzionato anche quando è stato somministrato per via orale a topi e in due scimmie cynomolgus su tre, il tutto senza effetti collaterali apparenti. “Si tratta della prima piccola molecola che induce l’emoglobina fetale senza danneggiare le cellule staminali”, ha precisato Bradner. Nonostante la promessa, il composto deve ancora affrontare delle sfide. Per cominciare, WIZ è prodotto in molti tipi di cellule oltre ai globuli rossi e sembra avere un ruolo nella regolazione dell’attività di numerosi geni. “Questo potrebbe renderlo un attore troppo ampio per poterlo reprimere in modo sicuro”, ha dichiarato Stuart Orkin, biologo delle cellule staminali presso il Dana-Farber Cancer Institute dell’Università di Harvard e ricercatore esperto di cellule falciformi non coinvolto nel nuovo lavoro. Ma Bradner osserva che il dWIZ-2 sembra avere un effetto maggiore nell’aumentare l’emoglobina fetale. Quindi, a prescindere dal fatto che il composto sperimentale di Novartis superi i test clinici, ha già contribuito a rivelare un nuovo modo di controllare quali tipi di emoglobina producono i globuli rossi. “E questo, di per sé, potrebbe gettare le basi per un futuro miglioramento dei farmaci contro la malattia”, ha concluso Bradner. (30Science.com)
Lucrezia Parpaglioni
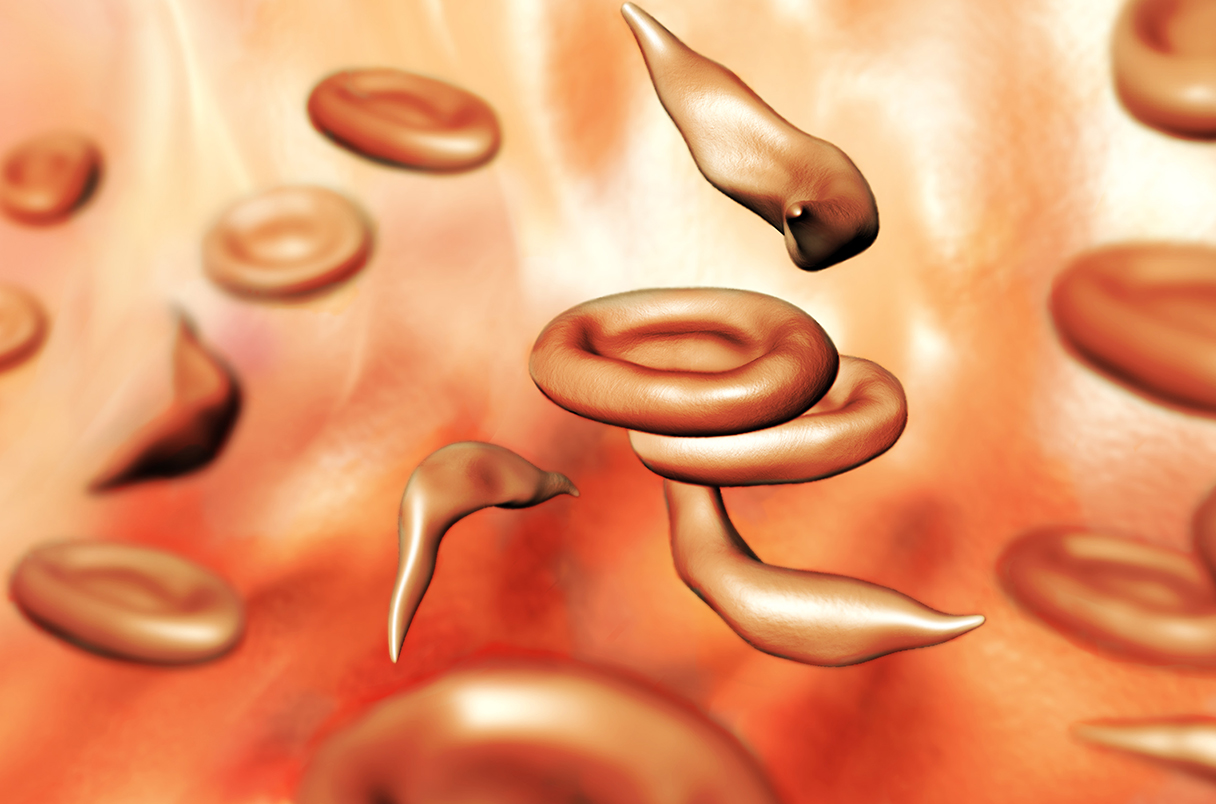
Una pillola promette di curare l’anemia falciforme
(9 Luglio 2024)

Lucrezia Parpaglioni
Sono nata nel 1992. Sono laureata in Media Comunicazione digitale e Giornalismo presso l'Università Sapienza di Roma. Durante il mio percorso di studi ho svolto un'attività di tirocinio presso l'ufficio stampa del Consiglio Nazionale delle Ricerche (CNR). Qui ho potuto confrontarmi con il mondo della scienza fatto di prove, scoperte e ricercatori. E devo ammettere che la cosa mi è piaciuta. D'altronde era prevedibile che chi ha da sempre come idolo Margherita Hack e Sheldon Cooper come spirito guida si appassionasse a questa realtà. Da qui la mia voglia di scrivere di scienza, di fare divulgazione e perché no? Dimostrare che la scienza può essere anche divertente.