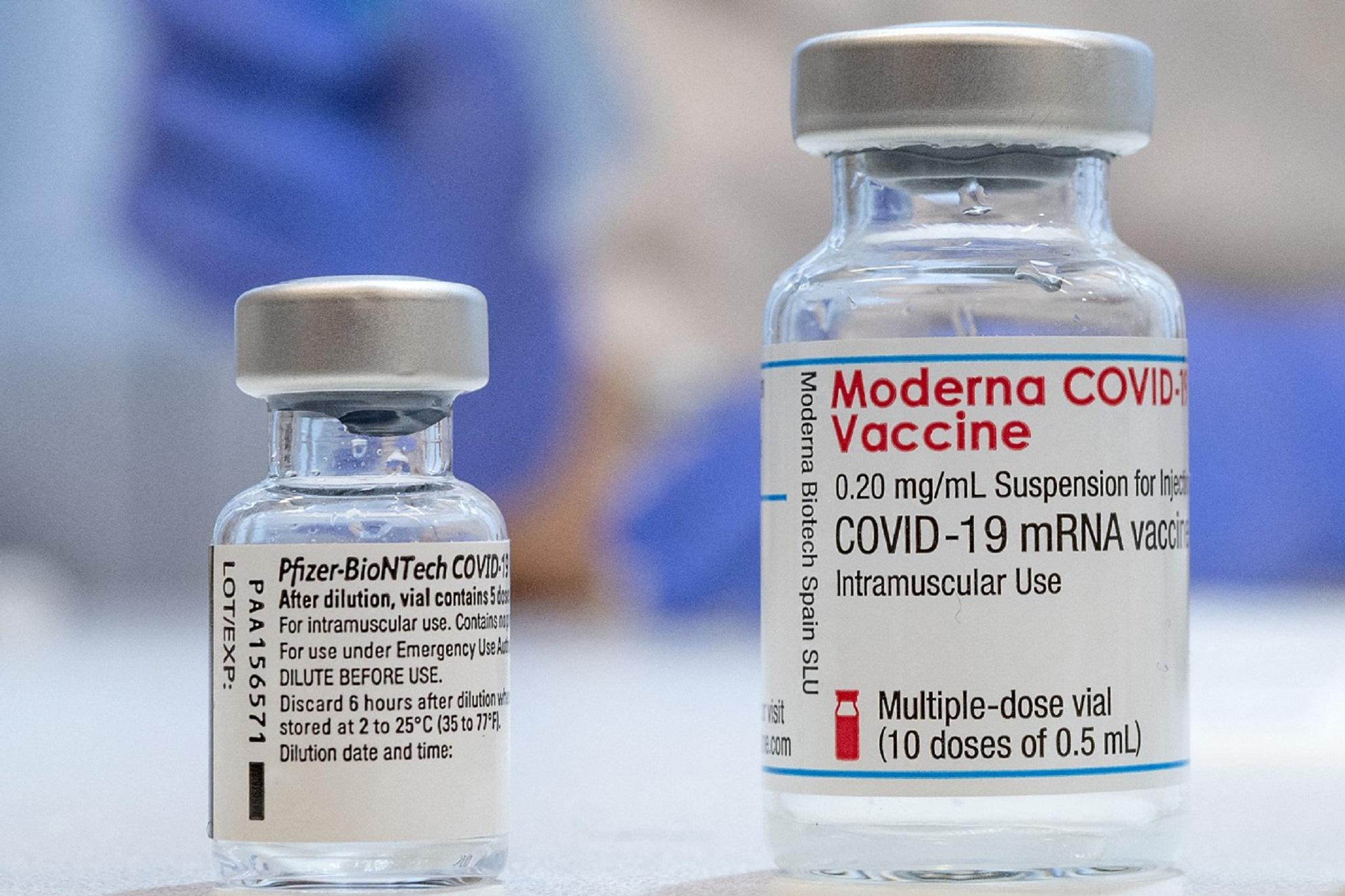(30Science.com) – Roma, 7 giu. – “Siamo lieti di annunciare che abbiamo presentato all’Agenzia Europea dei Medicinali (EMA) la richiesta di approvazione della commercializzazione condizionata del nostro vaccino contro il Covid-19 (mRNA-1273) per l’uso negli adolescenti”, ha dichiarato Stéphane Bancel, Chief Executive Officer di Moderna. “Siamo incoraggiati dal fatto che il vaccino si è dimostrato essere altamente efficace nel prevenire l’infezione da COVID-19 e SARS-CoV-2 negli adolescenti. Abbiamo inoltre richiesto l’autorizzazione a Health Canada e richiederemo un’autorizzazione d’emergenza alla FDA degli Stati Uniti e alle agenzie di regolamentazione di tutto il mondo per questa importante fascia di popolazione. Restiamo impegnati a fare la nostra parte per aiutare a porre fine alla pandemia di COVID-19”. La richiesta è basata sullo studio di fase 2/3 di mRNA-1273 in adolescenti di età compresa tra 12 e meno di 18 anni negli Stati Uniti. Nei quasi 2.500 adolescenti che lo hanno ricevuto, è stata osservata un’efficacia del vaccino pari al 100% quando si è utilizzata la stessa definizione di caso dello studio di fase 3 COVE negli adulti. È stata osservata un’efficacia del vaccino del 93% nei partecipanti sieronegativi a partire da 14 giorni dopo la prima dose utilizzando la definizione di caso secondaria di COVID-19 utilizzata dal Centres for Disease Control and Prevention (CDC), che ha testato una malattia più lieve. Il vaccino COVID-19 di Moderna è stato generalmente ben tollerato con un profilo di sicurezza e tollerabilità generalmente coerente con lo studio di fase 3 COVE negli adulti.

30Science.com
Agenzia di stampa quotidiana specializzata su temi di scienza, ambiente, natura, salute, società, mobilità e tecnologia. Ogni giorno produciamo una rassegna stampa delle principali riviste scientifiche internazionali e quattro notiziari tematici: Scienza, Clima & Natura, Salute, Nuova Mobilità e Ricerca Italiana
contatti:
redazione@30science.com
+ 39 3492419582